国家食品药品监督管理总局医疗器械技术审评中心2017年下半年公开招聘简章
一、单位介绍
国家食品药品监督管理总局医疗器械技术审评中心成立于1996年,是国家食品药品监督管理总局直属事业单位(正局级),现办公地点为北京市海淀区气象路50号院1号楼。
本中心主要负责对境内第三类医疗器械产品和进口医疗器械产品进行技术审评;参与起草医疗器械注册管理相关法规规章和规范性文件。内设11个机构,其中审评部门6个,综合管理部门5个,具体可参见中心官网www.cmde.org.cn
医疗器械技术审评中心内设机构图
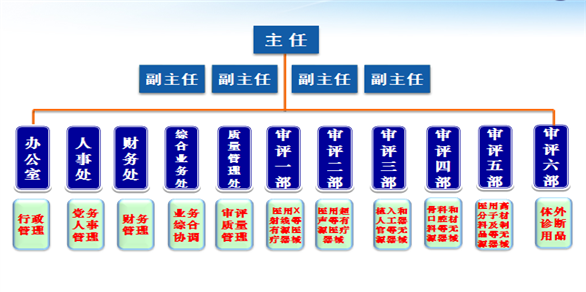
二、发展愿景
医疗器械与药品一样是一种特殊商品,其质量安全和创新发展,关乎公众健康安全和社会和谐稳定,是建设健康中国的重要保障。当前,我国医疗器械产业快速发展,创新创业方兴未艾,现有生产企业1.5万余家,经营企业20余万家,多学科交叉科技创新体系已经形成,产业规模不断壮大,呈现集群发展态势,成为全球医疗器械的主要生产和进出口基地。
为了加强对医疗器械的监督管理,保证产品安全、有效,我国对医疗器械产品实行上市前审查注册制度。中心是唯一一家国家级技术审评机构,经过20年的发展,在机构、队伍、审评建设等方面积极推进工作,年审评量过万件,为我国的医疗器械注册管理提供了坚强的技术支撑,为保障公众用械安全有效和促进产业健康发展发挥了积极作用。
2015年以来,为贯彻《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号),中心正在全面推进审评体制、机制、人事、薪酬等改革。建设高素质的审评人才队伍是此次改革的重要内容。为实现这一目标,中心积极变革人才引进机制,面向社会公开招聘合同制工作人员,实行岗位聘用管理,并建立起较为完善的考核晋升渠道、人才培养体系和薪酬管理体系,为人才成长与发展提供了良好平台。
2017年10月,中共中央办公厅、国务院办公厅联合印发了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,这是继2015年44号文件之后,又一个深化药品医疗器械审评审批制度改革的纲领性文件,对我国医药产业创新发展以及医疗器械审评审批改革发展具有里程碑意义。
医疗器械产业蓬勃发展,医疗器械审评事业任重道远。医疗器械技术审评中心将抓住改革时机,坚持以人民为中心的发展思想,认真贯彻落实习近平总书记关于食品药品监管“四个最严”的重要指示以及党中央、国务院关于鼓励医疗器械创新的部署和要求,全面深化推进医疗器械审评审批改革。欢迎各位有志青年,加入国家食品药品监督管理总局医疗器械技术审评中心,为公众用械安全和我国医疗器械产业发展贡献力量。
三、招聘条件、流程和要求
详见《国家食品药品监督管理总局医疗器械技术审评中心2017年下半年审评工作人员公开招聘公告》
附件1:岗位需求信息表
附件2:应聘报名表(应届毕业生)
附件3:报名人员信息登记表